Как составлять химические. Составление химических формул
В уроке 13 «» из курса «Химия для чайников » рассмотрим для чего нужны химические уравнения; научимся уравнивать химические реакции, путем правильной расстановки коэффициентов. Данный урок потребует от вас знания химических основ из прошлых уроков. Обязательно прочитайте об элементном анализе, где подробно рассмотрены эмпирические формулы и анализ химических веществ.
В результате реакции горения метана CH 4 в кислороде O 2 образуются диоксид углерода CO 2 и вода H 2 O. Эта реакция может быть описана химическим уравнением :
- CH 4 + O 2 → CO 2 + H 2 O (1)
Попробуем извлечь из химического уравнения больше сведений, чем просто указание продуктов и реагентов реакции. Химичекое уравнение (1) является НЕполным и потому не дает никаких сведений о том, сколько молекул O 2 расходуется в расчете на 1 молекулу CH 4 и сколько молекул CO 2 и H2 O получается в результате. Но если записать перед соответствующими молекулярными формулами численные коэффициенты, которые укажут сколько молекул каждого сорта принимает участие в реакции, то мы получим полное химическое уравнение реакции.
Для того, чтобы завершить составление химического уравнения (1), нужно помнить одно простое правило: в левой и правой частях уравнения должно присутствовать одинаковое число атомов каждого сорта, поскольку в ходе химической реакции не возникает новых атомов и не происходит уничтожение имевшихся. Данное правило основывается на законе сохранения массы, который мы рассмотрели в начале главы.
Нужно для того, чтобы из простого химического уравнения получить полное. Итак, перейдем к непосредственному уравниванию реакции (1): еще раз взгляните на химическое уравнение, в точности на атомы и молекулы в правой и левой части. Нетрудно заметить, что в реакции участвуют атомы трех сортов: углерод C, водород H и кислород O. Давайте подсчитаем и сравним количество атомов каждого сорта в правой и левой части химического уравнения.
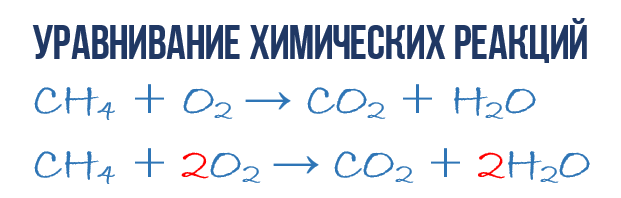
Начнем с углерода. В левой части один атом С входит в состав молекулы CH 4 , а в правой части один атом С входит в состав CO 2 . Таким образом в левой и в правой части количество атомов углерода совпадает, поэтому его мы оставляем в покое. Но для наглядности поставим коэффициент 1 перед молекулами с углеродом, хоть это и не обязательно:
- 1CH 4 + O 2 → 1CO 2 + H 2 O (2)
Затем переходим к подсчету атомов водорода H. В левой части присутствуют 4 атома H (в количественном смысле H 4 = 4H) в составе молекулы CH 4 , а в правой – всего 2 атома H в составе молекулы H 2 O, что в два раза меньше чем в левой части химического уравнения (2). Будем уравнивать! Для этого поставим коэффициент 2 перед молекулой H 2 O. Вот теперь у нас и в реагентах и в продуктах будет по 4 молекулы водорода H:
- 1CH 4 + O 2 → 1CO 2 + 2H 2 O (3)
Обратите свое внимание, что коэффициент 2, который мы записали перед молекулой воды H 2 O для уравнивания водорода H, увеличивает в 2 раза все атомы, входящие в ее состав, т.е 2H 2 O означает 4H и 2O. Ладно, с этим вроде бы разобрались, осталось подсчитать и сравнить количество атомов кислорода O в химическом уравнении (3). Сразу бросается в глаза, что в левой части атомов O ровно в 2 раза меньше чем в правой. Теперь-то вы уже и сами умеете уравнивать химические уравнения, поэтому сразу запишу финальный результат:
- 1CH 4 + 2O 2 → 1CO 2 + 2H 2 O или СH 4 + 2O 2 → CO 2 + 2H 2 O (4)
Как видите, уравнивание химических реакций не такая уж и мудреная штука, и важна здесь не химия, а математика. Уравнение (4) называется полным уравнением химической реакции, потому что в нем соблюдается закон сохранения массы, т.е. число атомов каждого сорта, вступающих в реакцию, точно совпадает с числом атомов данного сорта по завершении реакции. В каждой части этого полного химического уравнения содержится по 1 атому углерода, по 4 атома водорода и по 4 атома кислорода. Однако стоит понимать пару важных моментов: химическая реакция — это сложная последовательность отдельных промежуточных стадий, и потому нельзя к примеру истолковывать уравнение (4) в том смысле, что 1 молекула метана должна одновременно столкнуться с 2 молекулами кислорода. Процессы происходящие при образовании продуктов реакции гораздо сложнее. Второй момент: полное уравнение реакции ничего не говорит нам о ее молекулярном механизме, т.е о последовательности событий, которые происходят на молекулярном уровне при ее протекании.
Коэффициенты в уравнениях химических реакций
Еще один наглядный пример того, как правильно расставить коэффициенты в уравнениях химических реакций: Тринитротолуол (ТНТ) C 7 H 5 N 3 O 6 энергично соединяется с кислородом, образуя H 2 O, CO 2 и N 2 . Запишем уравнение реакции, которое будем уравнивать:
- C 7 H 5 N 3 O 6 + O 2 → CO 2 + H 2 O + N 2 (5)
Проще составлять полное уравнение, исходя из двух молекул ТНТ, так как в левой части содержится нечетное число атомов водорода и азота, а в правой — четное:
- 2C 7 H 5 N 3 O 6 + O 2 → CO 2 + H 2 O + N 2 (6)
Тогда ясно, что 14 атомов углерода, 10 атомов водорода и 6 атомов азота должны превратиться в 14 молекул диоксида углерода, 5 молекул воды и 3 молекулы азота:
- 2C 7 H 5 N 3 O 6 + O 2 → 14CO 2 + 5H 2 O + 3N 2 (7)
Теперь в обеих частях содержится одинаковое число всех атомов, кроме кислорода. Из 33 атомов кислорода, имеющихся в правой части уравнения, 12 поставляются двумя исходными молекулами ТНТ, а остальные 21 должны быть поставлены 10,5 молекулами O 2 . Таким образом полное химическое уравнение будет иметь вид:
- 2C 7 H 5 N 3 O 6 + 10,5O 2 → 14CO 2 + 5H 2 O + 3N 2 (8)
Можно умножить обе части на 2 и избавиться от нецелочисленного коэффициента 10,5:
- 4C 7 H 5 N 3 O 6 + 21O 2 → 28CO 2 + 10H 2 O + 6N 2 (9)
Но этого можно и не делать, поскольку все коэффициенты уравнения не обязательно должны быть целочисленными. Правильнее даже составить уравнение, исходя из одной молекулы ТНТ:
- C 7 H 5 N 3 O 6 + 5,25O 2 → 7CO 2 + 2,5H 2 O + 1,5N 2 (10)
Полное химическое уравнение (9) несет в себе много информации. Прежде всего оно указывает исходные вещества — реагенты , а также продукты реакции. Кроме того, оно показывает, что в ходе реакции индивидуально сохраняются все атомы каждого сорта. Если умножить обе части уравнения (9) на число Авогадро N A =6,022·10 23 , мы сможем утверждать, что 4 моля ТНТ реагируют с 21 молями O 2 с образованием 28 молей CO 2 , 10 молей H 2 O и 6 молей N 2 .
Есть еще одна фишка. При помощи таблицы Менделеева определяем молекулярные массы всех этих веществ:
- C 7 H 5 N 3 O 6 = 227,13 г/моль
- O2 = 31,999 г/моль
- CO2 = 44,010 г/моль
- H2 O = 18,015 г/моль
- N2 = 28,013 г/моль
Теперь уравнение 9 укажет еще, что 4·227,13 г = 908,52 г ТНТ требуют для осуществления полной реакции 21·31,999 г = 671,98 г кислорода и в результате образуется 28·44,010 г = 1232,3 г CO 2 , 10·18,015 г = 180,15 г H 2 O и 6·28,013 г = 168,08 г N 2 . Проверим, выполняется ли в этой реакции закон сохранения массы:
| Реагенты | Продукты | |
| 908,52 г ТНТ | 1232,3 г CO2 | |
| 671,98 г CO2 | 180,15 г H2 O | |
| 168,08 г N2 | ||
| Итого | 1580,5 г | 1580,5 г |
Но необязательно в химической реакции должны участвовать индивидуальные молекулы. Например, реакция известняка CaCO3 и соляной кислоты HCl, с образованием водного раствора хлорида кальция CaCl2 и диоксида углерода CO2 :
- CaCO 3 + 2HCl → CaCl 2 + CO 2 + H 2 O (11)
Химическое уравнение (11) описывает реакцию карбоната кальция CaCO 3 (известняка) и хлористоводородной кислоты HCl с образованием водного раствора хлорида кальция CaCl 2 и диоксида углерода CO 2 . Это уравнение полное, так как число атомов каждого сорта в его левой и правой частях одинаково.
Смысл этого уравнения на макроскопическом (молярном) уровне таков: 1 моль или 100,09 г CaCO 3 требует для осуществления полной реакции 2 моля или 72,92 г HCl, в результате чего получается по 1 молю CaCl 2 (110,99 г/моль), CO 2 (44,01 г/моль) и H 2 O (18,02 г/моль). По этим численным данным нетрудно убедиться, что в данной реакции выполняется закон сохранения массы.
Интерпретация уравнения (11) на микроскопическом (молекулярном) уровне не столь очевидна, поскольку карбонат кальция представляет собой соль, а не молекулярное соединение, а потому нельзя понимать химическое уравнение (11) в том смысле, что 1 молекула карбоната кальция CaCO 3 реагирует с 2 молекулами HCl. Тем более молекула HCl в растворе вообще диссоциирует (распадается) на ионы H + и Cl — . Таким образом более правильным описанием того, что происходит в этой реакции на молекулярном уровне, дает уравнение:
- CaCO 3 (тв.) + 2H + (водн.) → Ca 2+ (водн.) + CO 2 (г.) + H 2 O(ж.) (12)
Здесь в скобках сокращенно указано физическое состояние каждого сорта частиц (тв. — твердое, водн. — гидратированный ион в водном растворе, г. — газ, ж. — жидкость).
Уравнение (12) показывает, что твердый CaCO 3 реагирует с двумя гидратированными ионами H + , образуя при этом положительный ион Ca 2+ , CO 2 и H 2 O. Уравнение (12) как и другие полные химические уравнения не дает представления о молекулярном механизме реакции и менее удобно для подсчета количества веществ, однако, оно дает лучшее описание происходящего на микроскопическом уровне.
Закрепите полученные знания о составлении химических уравнений, самостоятельно разобрав пример с решением:
Надеюсь из урока 13 «Составление химических уравнений » вы узнали для себя что-то новое. Если у вас возникли вопросы, пишите их в комментарии.
§ 1 Валентность химических элементов
В свое время, состав всех веществ был установлен на основании данных эксперимента. Однако можно составлять химические формулы, не прибегая к предварительному выполнению сложных опытов, требующих длительной, кропотливой работы.
Если сравнить между собой формулы таких веществ, как вода H2O, оксид кальция СаО, оксид алюминия Al2O3, оксид углерода СО2, оксид фосфора Р2О5, оксид серы SО3 и оксид хлора Cl2О7, то можно заметить, что кислород во всех этих соединениях присоединяет к себе неодинаковое число атомов других химических элементов.
Для определения состава бинарных или двухэлементных, то есть состоящих из атомов двух химических элементов соединений, и составления их формул, достаточно знать валентность химических элементов.
Валентность (от латинского слова Valentia - «сила») - свойство атома химического элемента присоединять или замещать определённое число атомов другого химического элемента
Поскольку атомы в молекуле соединены между собой химическими связями, валентность определяется числом простых (одинарных) химических связей, которые данный атом образует с другими атомами.
§ 2 Определение валентности по формулам соединений
Как это можно представить себе, если не прибегать к теории строения атома? Каждый атом имеет определенное число потенциальных химических связей - валентных возможностей.

Например, водород - одну, кислород и кальций - по две, алюминий - три, углерод - четыре, фосфор - пять, сера - шесть, хлор - семь. Соединяться друг с другом эти атомы могут, только используя эти самые валентные возможности.
Поэтому атомы химических элементов и образуют соединения, подчиняясь закону постоянства состава.
Закон постоянства состава утверждает, что вещества, независимо от нахождения в природе или способа получения их в лаборатории, всегда имеют один и тот же состав.

Способность элементов проявлять то или иное значение валентности определяется строением их атомов. Поскольку строение атомов обычно изучается позднее, научимся определять валентность, исходя из положения элементов в периодической системе.
Для этого следует учитывать, что каждая группа (вертикальный столбец) элементов состоит из двух подгрупп: главной А и побочной В.

Элементы-металлы, располагающиеся в главных подгруппах I и II групп, проявляют постоянную валентность, равную номеру группы. Это же относится и к алюминию (III группа). А вот металлические элементы IV группы (главная подгруппа) олово и свинец служат исключением и проявляют переменную валентность, численно равную 2 и 4. Длямногих металлов побочных подгрупп также характерно наличие переменной валентности, однако высшее значение валентности обычно равно номеру группы!

Большая часть неметаллов, располагающихся в главных подгруппах групп с четвёртой по седьмую, проявляет переменную валентность. В ряду возможных значений валентностей неметаллов следует выделять высшую и низшую. Высшая валентность равна номеру группы, низшая - разности, полученной вычитанием числа, равного номеру группы, из числа 8. Например: высшая валентность элемента фосфора, стоящего в V группе, равна 5,
низшая: 8-5=3. Следовательно, валентность фосфора переменная - 3 и 5. Следует помнить, что высшая валентность неметаллов проявляется только в соединениях с кислородом, а низшая - в соединениях с металлами и водородом. Валентность водорода всегда во всех соединениях равна 1, валентность кислорода всегда 2.
§ 3 Составление химических формул по валентности
Для составления формул сложных веществ, состоящих из атомов двух неметаллов, следует учитывать, что высшую валентность проявит тот элемент, который стоит в периодической системе левее или ниже, а низшую - соответственно тот, который стоит правее или выше.
Составляем формулы и названия веществ по валентности, используя следующий алгоритм:
1. записываем знаки элементов (по наличию) в порядке: металл, водород, неметалл, кислород;
2. расставляем значения валентностей элементов по периодической системе химических элементов;
3. находим наименьшее общее кратное значений валентностей (наименьшее число, которое делится на оба значения валентностей), делим его на валентность каждого элемента, получаем и записываем индекс;
4. называем вещество. К латинскому корню второго элемента прибавляем суффикс ид, указываем русское название первого элемента и его валентность, если она не постоянная.

Составим формулу и название для вещества, состоящего из атомов фосфора и кислорода:
1. записываем знаки Р и О;
2. валентность фосфора высшая, равна 5, валентность кислорода, как и во всех соединениях равна 2;
3. наименьшее общее кратное 10
10/5=2, пишем индекс у знака Р
10/2=5, пишем индекс у знака О
получилось Р2О5;
4. назовем вещество: корень латинского названия кислорода «оксигениум» окс, к нему прибавляем суффикс ид, получаем оксид. Русское название первого элемента - фосфор, валентность его переменная, равная 5. Получилось название «оксид фосфора 5».
§ 4 Определение названия вещества по химической формуле
Таким образом, при составлении названия вещества, имеющего определенную химическую формулу, необходимо указывать валентность, а чтобы ее указать, необходимо определить. По периодической системе это получается не всегда. Определить валентность и составить название веществаможно, используя алгоритм:
1. указать валентность известного элемента;
2. умножить указанную валентность на соответствующий индекс;
3. полученный результат делим на индекс элемента с неизвестной валентностью;
4. называем вещество. К латинскому корню второго элемента прибавляем суффикс ид, указываем русское название первого элемента и его валентность.
Определим валентность и составим название вещества, имеющего формулу CrO3:
1. валентность кислорода постоянна и равна 2;
3. 6/1=6. Валентность хрома равна 6;
4. название вещества - оксид хрома 6.
Теперь научимся составлять формулу по названию вещества
1. записываем знаки химических элементов в нужном порядке;
2. указываем валентности, обращая внимание на название. Если валентность первого элемента переменная, она будет указана. Валентность второго элемента - низшая;
3. находим наименьшее общее кратное значений валентностей (наименьшее число, которое делится на оба значения валентностей), делим его на валентность каждого элемента, получаем и записываем индекс.

Определим формулу оксида серы:
1. записываем знаки S и О.
2. валентность серы равна 4, валентность кислорода, как и во всех соединениях - два.
3. наименьшее общее кратное 4
4/2=2, пишем индекс у знака О
4/4=1, пишем индекс у знака S;
4. получилось SО2.
Список использованной литературы:
- Н.Е. Кузнецова. Химия. 8 класс. Учебник для общеобразовательных учреждений. – М. Вентана-Граф, 2012.
Использованные изображения:
«Знание шрифтов – одно из самых элементарных требований, предъявляемых к сыщику!», - так наставлял когда-то великий Шерлок Холмс своего друга и летописца доктора Ватсона. Аналогично этому, можно смело сказать: «Знание того, как составляются химические формулы – одно из самых элементарных требований, предъявляемых к химику!» В самом деле, как можно рассуждать о превращениях веществ, не умея составлять их формулы ?
Вам понадобится
- - таблица Менделеева.
Инструкция
Тут вам надо опираться на такое понятие, как « », то есть способность атома одного вещества присоединять к себе определенное количество атомов другого вещества. Валентность любого элемента можно узнать, заглянув в таблицу Менделеева и помня некоторые общие правила.
Валентность металла, находящегося в «главной» подгруппе, равна номеру группы. Например, щелочные металлы литий, натрий, калий и т.д. – одновалентные, щелочноземельные кальций, стронций, барий и т.д. – двухвалентные.
Неметаллы имеют две валентности – высшую (которая равна номеру группы) и низшую (которую определяют, вычитая из 8 номер группы). В соединениях с металлами неметаллы имеют низшую валентность!
Если два неметалла соединяются между собой, то низшую валентность проявляет тот неметалл, который находится в Таблице Менделеева правее и выше. Фтор является исключением из этих правил, и всегда проявляет валентность, равную 1.
Необходимо также помнить, что в соединениях, состоящих из двух элементов, общее число валентностей одного элемента всегда должно быть равно общему количеству валентностей другого элемента!
Запомнив эти весьма несложные положения, вы сможете легко составлять химические формулы . Например, какова будет формула фосфорного ангидрида, то есть оксида фосфора? Во-первых, сразу возьмите на заметку: и фосфор, и кислород – неметаллы. Во-вторых, смотрите в таблицу Менделеева. Фосфор располагается в пятой группе, кислород – в шестой. Следовательно, низшую валентность в этом соединении проявит кислород, и она будет равна 2 (8 – 6 = 2). Валентность фосфора, соответственно, будет равна 5.
Какие же коэффициенты надо подставить и к фосфору, и к кислороду, чтобы соблюсти правило: сумма валентностей одного элемента должна равняться сумме валентностей второго? Легко можно увидеть, что для цифр 2 и 5 наименьшее общее кратное - 10. Следовательно, искомая формула фосфорного ангидрида такова: Р2О5.
Ну, а какова будет формула азида лития, то есть, вещества, образованного неметаллом азотом и щелочным металлом литием? Литий имеет валентность, равную 1. Азот, располагаясь в 5 группе, может иметь высшую валентность, равную 5, и низшую, равную 3. А поскольку в соединениях с металлами неметаллы имеют низшую валентность, легко вывести формулу этого соединения: Li3N.
Внимание, только СЕГОДНЯ!
Все интересное
Периодическая система химических элементов – это уникальный справочный материал, который нужно правильно «читать», а затем воспользоваться полученной информацией. Помимо этого таблица Д.И. Менделеева считается разрешенным материалом на…
Валентность – один из основных терминов, употребляемых в теории химического строения. Это понятие определяет способность атома образовывать химические связи и количественно представляет собой число связей, в которых он участвует. Инструкция …
Химическая формула – это условное обозначение, написанное с помощью определенных символов и характеризующее состав любого вещества. С помощью химической формулы вы можете увидеть, атомы каких элементов и в каких количествах входят в состав той или…
Валентность – важнейшее понятие химии. Физический смысл этого понятия стал ясен благодаря развитию учения о химической связи. Валентность атома определяется числом ковалентных связей, которыми он соединен с другими атомами. Инструкция 1Главную…
Валентность - это способность атома вступать во взаимодействие с другими атомами, образуя с ними химические связи. В создание теории валентности внесли большой вклад многие ученые, прежде всего, немец Кекуле и наш соотечественник Бутлеров.…
Количество известных химических соединений исчисляется миллионами. По мере развития науки и производства их будет становиться все больше, и запомнить их все не в состоянии даже самый квалифицированный специалист. Но можно научиться самим составлять…
Фосфор – химический элемент, имеющий 15-й порядковый номер в Таблице Менделеева. Он расположен в ее V группе. Классический неметалл, открытый алхимиком Брандом в 1669-м году. Существует три основных модификации фосфора: красный (входящий в состав…
Химическая формула – это запись, сделанная с использованием общепринятых символов, которая характеризует состав молекулы какого-либо вещества. Например, формула всем известной серной кислоты – H2SO4. Легко можно увидеть, что каждая молекула серной…
Валентность - это способность химических элементов удерживать определенное количество атомов других элементов. В то же самое время, это число связей, образуемое данным атомом с другими атомами. Определить валентность достаточно просто. Инструкция …
Химия для каждого школьника начинается с таблицы Менделеева и фундаментальных законов. И уже только потом, уяснив для себя, что же изучает эта сложная наука, можно приступать к составлению химических формул. Для грамотной записи соединения нужно…
Оксиды – это сложные химические вещества, которые состоят из двух элементов. Одним из них является кислород. Оксиды в большинстве случаев бывают кислотными и основными. Как легко понять из названия, кислотные оксиды реагируют с основаниями, образуя…
Валентность химического элемента - это способность атома присоединять или замещать определенное число других атомов или атомных групп с образованием химической связи. Нужно помнить, что некоторые атомы одного и того же химического элемента могут…
В таблице 15 приведены названия часто встречающихся кислот, их молекулярные и структурные формулы, а также формульные единицы и названия соответствующих солей.
Таблица помогает составлять химические формулы солей бескислородных и кислородсодержащих кислот. Для образования химических формул солей надо атомы водорода в кислотах заменить на атомы металлов с учётом их валентности.
Приведённые названия кислот и солей соответствуют принятой международной номенклатуре.
Название бескислородных кислот образуются по правилам для бинарных соединений.
Названия солей начинаются с названия кислотного остатка в именительном падеже. Это название образуется из корня латинского названия химического элемента, образующего кислоту, и окончания "ат" или "ит" в случае солей кислородсодержащих кислот, для солей бескислородных кислот – "ид". Затем в солях бескислородных кислот называется металл в родительном падеже. Причём если атом металла может иметь разную валентность, то её отмечают римской цифрой (в скобках) после названия химического элемента (без пробела). Например, хлорид железа(II) и хлорид олова(IV).
Включение в таблицу названий молекулярных и структурных формул часто встречающихся кислот позволяет легко запомнить приведённые в ней сведения.
Названия кислот типа H n XO m составляют с учётом валентности (степени окисления) центрального атома:
– атом X имеет высшую (или единственную) валентность (степень окисления): H 2 SО 4 – серная; HNО 3 – азотная; Н 2 СО 3 – угольная;
– атом X имеет промежуточные степени окисления: H 2 SO 3 – сернистая; HNО 2 – азотистая; НСlО – хлорноватистая.
Таблица 15
Составление химических формул солей
ГЕНЕТИЧЕСКАЯ СВЯЗЬ КЛАССОВ
НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Таблица 16 показывает в виде схемы взаимосвязь неорганических веществ разных классов. Изучение свойств веществ показывает, что можно при помощи химических реакций переходить от простых веществ к сложным и от одних сложных веществ к другим. Связь между веществами разных классов, основанная на их взаимопревращениях и отражающая единство их происхождения, называется генетической .
Вещества по составу подразделяются на простые и сложные. Среди простых веществ различают металлы и неметаллы. Эти две группы веществ могут образовывать многочисленные сложные вещества. К основным классам неорганических соединений принадлежат оксиды, гидроксиды и соли. Связь между этими классами веществ обозначена при помощи стрелок.
По таблице можно проследить переходы металлов и неметаллов в оксиды и гидроксиды:
Эти две цепочки превращений аналогичны и роднят металлы и неметаллы.
Однако надо подчеркнуть, что простое вещество металл является родоначальником сложных веществ, обладающих оснóвными свойствами (оснóвных оксидов и оснований). Простое вещество неметалл выступает в качестве родоначальника сложных веществ, проявляющих кислотные свойства (кислотных оксидов и кислот).
Различие свойств кислотных и оснóвных оксидов, а также свойств кислот и оснований приводит к их взаимодействию друг с другом с образованием солей. Таким образом, соли генетически связаны с исходными веществами – металлами и неметаллами – посредством их оксидов и гидроксидов.
Так как соли представляют собой продукты реакций кислот и оснований, то по составу различают средние (нормальные), кислые и оснóвные соли. Кислые соли содержат в своём составе атомы водорода, оснóвные – гидроксогруппы. Названия кислых солей складываются из названий солей с прибавлением слова "гидро", а основных – "гидроксо".
Существуют также двойные соли (соли двух металлов), к ним относят, например, алюмокалиевые квасцы KA1(SО 4) 2 · 12Н 2 О, смешанные соли NаСl · NаF, СаВrСl, комплексные соли Nа 2 , К 3 , К 4 , включая кристаллогидраты СuSО 4 · 5Н 2 О (медный купорос), Nа 2 SО 4 · 10Н 2 О (глауберова соль)
Необходимо научиться составлять химические формулы гидроксидов (кислородсодержащих кислот и оснований) для атома элемента Э с валентностью "n". Гидроксиды получают по реакции присоединения воды к соответствующим оксидам. При этом не имеет значение, происходит ли эта реакция в реальных условиях. Например, химическую формулу угольной кислоты получают сложением всех атомов по уравнению реакции
СО 2 + Н 2 О = Н 2 СО 3 .
Химические формулы метафосфорной , пирофосфорной и ортофосфорной кислот составляют из формулы оксида фосфора(V)1 и соответственно одной, двух и трёх молекул воды:
Р 2 О 5 + Н 2 О = 2НРО 3 ;
Р 2 О 5 + 2Н 2 О = Н 4 Р 2 О 7 ;
Р 2 О 5 + 3Н 2 О = 2Н 3 РО 4 .
Приведённая схема взаимосвязи между классами неорганических веществ не охватывает всего многообразия химических соединений. В этой схеме в качестве бинарных веществ выступают оксиды,
Таблица 16
Химия – это наука о веществах, их свойствах и превращениях
.
То есть, если с окружающими нас веществами ничего не происходит, то это не относится к химии. Но что значит, «ничего не происходит»? Если в поле нас вдруг застала гроза, и мы все промокли, как говорится «до нитки», то это ли не превращение: ведь одежда была сухой, а стала мокрой.
Если, к примеру взять железный гвоздь, обработать его напильником, а затем собрать железные опилки (Fe ) , то это ли так же не превращение: был гвоздь – стал порошок. Но если после этого собрать прибор и провести получение кислорода (О 2) : нагреть перманганат калия (КМпО 4) и собрать в пробирку кислород, а затем в неё поместить раскалённые «до красна» эти железные опилки, то они вспыхнут ярким пламенем и после сгорания превратятся в порошок бурого цвета. И это так же превращение. Так где же химия? Несмотря на то, что в этих примерах меняется форма (железный гвоздь) и состояние одежды (сухая, мокрая) – это не превращения. Дело в том, что сам по себе гвоздь как был веществом (железо), так им и остался, несмотря на другую свою форму, а воду от дождя как впитала наша одежда, так потом его и испарила в атмосферу. Сама вода не изменилась. Так что же такое превращения с точки зрения химии?
Превращениями с точки зрения химии называются такие явления, которые сопровождаются изменением состава вещества. Возьмём в качестве примера тот же гвоздь. Не важно, какую форму он принял после обработки напильником, но после того как собранные от него железные опилки поместили в атмосферу кислорода - он превратился в оксид железа (Fe 2 O 3 ) . Значит, что-то всё-таки изменилось? Да, изменилось. Было вещество гвоздь, но под воздействием кислорода сформировалось новое вещество – оксид элемента железа. Молекулярное уравнение этого превращения можно отобразить следующими химическими символами:
4Fe + 3O 2 = 2Fe 2 O 3 (1)
Для непосвящённого в химии человека сразу возникают вопросы. Что такое «молекулярное уравнение», что такое Fe? Почему поставлены цифры «4», «3», «2»? Что такое маленькие цифры «2» и «3» в формуле Fe 2 O 3 ? Это значит, наступило время во всём разобраться по порядку.
Знаки химических элементов.
Несмотря на то, что химию начинают изучать в 8-м классе, а некоторые даже раньше, многим известен великий русский химик Д. И. Менделеев. И конечно же, его знаменитая «Периодическая система химических элементов». Иначе, проще, её называют «Таблица Менделеева».
В этой таблице, в соответствующем порядке, располагаются элементы. К настоящему времени их известно около 120. Названия многих элементов нам были известны ещё давно. Это: железо, алюминий, кислород, углерод, золото, кремний. Раньше мы не задумываясь применяли эти слова, отождествляя их с предметами: железный болт, алюминиевая проволока, кислород в атмосфере, золотое кольцо и т.д. и т.д. Но на самом деле все эти вещества (болт, проволока, кольцо) состоят из соответствующих им элементов. Весь парадокс состоит в том, что элемент нельзя потрогать, взять в руки. Как же так? В таблице Менделеева они есть, а взять их нельзя! Да, именно так. Химический элемент – это абстрактное (то есть отвлечённое) понятие, и используется в химии, впрочем как и в других науках, для расчётов, составления уравнений, при решении задач. Каждый элемент отличается от другого тем, что для него характерна своя электронная конфигурация атома. Количество протонов в ядре атома равно количеству электронов в его орбиталях. К примеру, водород – элемент №1. Его атом состоит из 1-го протона и 1-го электрона. Гелий – элемент №2. Его атом состоит из 2-х протонов и 2-х электронов. Литий – элемент №3. Его атом состоит из 3-х протонов и 3-х электронов. Дармштадтий – элемент №110. Его атом состоит из 110-и протонов и 110-и электронов.
Каждый элемент обозначается определённым символом, латинскими буквами, и имеет определённое прочтение в переводе с латинского. Например, водород имеет символ «Н» , читается как «гидрогениум» или «аш». Кремний имеет символ «Si» читается как «силициум». Ртуть имеет символ «Нg» и читается как «гидраргирум». И так далее. Все эти обозначения можно найти в любом учебнике химии за 8-й класс. Для нас сейчас главное уяснить то, что при составлении химических уравнений, необходимо оперировать указанными символами элементов.
Простые и сложные вещества.
Обозначая единичными символами химических элементов различные вещества (Hg ртуть , Fe железо , Cu медь , Zn цинк , Al алюминий ) мы по сути обозначаем простые вещества, то есть вещества, состоящие из атомов одного вида (содержащие одно и то же количество протонов и нейтронов в атоме). Например, если во взаимодействие вступают вещества железо и сера, то уравнение примет следующую форму записи:
Fe + S = FeS (2)
К простым веществам относятся металлы (Ва, К, Na, Mg, Ag), а так же неметаллы (S, P, Si, Cl 2 , N 2 , O 2 , H 2). Причём следует обратить
особое внимание на то, что все металлы обозначаются единичными символами: К, Ва, Са, Аl, V, Mg и т.д., а неметаллы – либо простыми символами: C,S,P или могут иметь различные индексы, которые указывают на их молекулярное строение: H 2 , Сl 2 , О 2 , J 2 , P 4 , S 8 . В дальнейшем это будет иметь очень большое значение при составлении уравнений. Совсем не трудно догадаться, что сложными веществами являются вещества, образованные из атомов разного вида, например,
1). Оксиды:
оксид алюминия
Al 2 O 3 ,  оксид натрия
Na 2 O,
оксид натрия
Na 2 O,
оксид меди
CuO,
оксид цинка
ZnO,
оксид титана
Ti 2 O 3 ,
угарный газ
или оксид углерода (+2)
CO,
оксид серы (+6)
SO 3
2). Основания:
гидроксид железа
(+3) Fe(OH) 3 ,
гидроксид меди
Cu(OH) 2 ,
гидроксид калия или щёлочь калия
КOH,
гидроксид натрия
NaOH.
3). Кислоты:
соляная кислота
HCl,
сернистая кислота
H 2 SO 3 ,
азотная кислота
HNO 3
4). Соли:
тиосульфат натрия
Na 2 S 2 O 3 ,
сульфат натрия
или глауберова соль
Na 2 SO 4 ,
карбонат кальция
или известняк
СаCO 3,
хлорид меди
CuCl 2
5). Органические вещества:
ацетат натрия
СН 3 СООNa,
метан
СН 4 ,
ацетилен
С 2 Н 2 ,
глюкоза
С 6 Н 12 О 6
Наконец, после того как мы выяснили структуру различных веществ, можно приступать к составлению химических уравнений.
Химическое уравнение.
Само слово «уравнение» производное от слова «уравнять», т.е. разделить нечто на равные части. В математике уравнения составляют чуть ли не самую сущность этой науки. К примеру, можно привести такое простое уравнение, в котором левая и правая части будут равны «2»:
40: (9 + 11) = (50 х 2) : (80 – 30);
И в химических уравнениях тот же принцип: левая и правая части уравнения должны соответствовать одинаковым количествам атомов, участвующим в них элементов. Или, если приводится ионное уравнение, то в нём число частиц так же должно соответствовать этому требованию. Химическим уравнением называется условная запись химической реакции с помощью химических формул и математических знаков. Химическое уравнение по своей сути отражает ту или иную химическую реакцию, то есть процесс взаимодействия веществ, в процессе которых возникают новые вещества. Например, необходимо написать молекулярное уравнение реакции, в которой принимают участие хлорид бария ВаСl 2 и серная кислота H 2 SO 4. В результате этой реакции образуется нерастворимый осадок – сульфат бария ВаSO 4 и соляная кислота НСl:
ВаСl 2 + H 2 SO 4 = BaSO 4 + 2НСl (3)
Прежде всего необходимо уяснить, что большая цифра «2», стоящая перед веществом НСlназывается коэффициентом, а малые цифры «2», «4» под формулами ВаСl 2 , H 2 SO 4 ,BaSO 4 называются индексами. И коэффициенты и индексы в химических уравнениях выполняют роль множителей, а не слагаемых. Что бы правильно записать химическое уравнение, необходимо расставить коэффициенты в уравнении реакции . Теперь приступим к подсчёту атомов элементов в левой и правой частях уравнения. В левой части уравнения: в веществе ВаСl 2 содержатся 1 атом бария (Ва), 2 атома хлора (Сl). В веществе H 2 SO 4: 2 атома водорода (Н), 1 атом серы (S) и 4 атома кислорода (О) . В правой части уравнения: в веществе BaSO 4 1 атом бария (Ва) 1 атом серы (S) и 4 атома кислорода (О), в веществе НСl: 1 атом водорода (Н) и 1 атом хлора (Сl). Откуда следует, что в правой части уравнения количество атомов водорода и хлора вдвое меньше, чем в левой части. Следовательно, перед формулой НСl в правой части уравнения необходимо поставить коэффициент «2». Если теперь сложить количества атомов элементов, участвующих в данной реакции, и слева и справа, то получим следующий баланс:

В обеих частях уравнения количества атомов элементов, участвующих в реакции, равны, следовательно оно составлено правильно.

Химические уравнение и химические реакции
Как мы уже выяснили, химические уравнения являются отражением химических реакций. Химическими реакциями называются такие явления, в процессе которых происходит превращение одних веществ в другие. Среди их многообразия можно выделить два основных типа:
1). Реакции соединения
2). Реакции разложения.
В подавляющем своём большинстве химические реакции принадлежат к реакциям присоединения, поскольку с отдельно взятым веществом редко могут происходить изменения в его составе, если оно не подвергается воздействиям извне (растворению, нагреванию, действию света). Ничто так не характеризует химическое явление, или реакцию, как изменения, происходящие при взаимодействии двух и более веществ. Такие явления могут осуществляться самопроизвольно и сопровождаться повышением или понижением температуры, световыми эффектами, изменением цвета, образованием осадка, выделением газообразных продуктов, шумом.
Для наглядности приведём несколько уравнений, отражающих процессы реакций соединения, в процессе которых получаются хлорид натрия (NaCl), хлорид цинка (ZnCl 2), осадок хлорида серебра (AgCl), хлорид алюминия (AlCl 3)
Cl 2 + 2Nа = 2NaCl (4)
СuCl 2 + Zn= ZnCl 2 + Сu (5)
AgNO 3 + КCl = AgCl + 2KNO 3 (6)
3HCl + Al(OH) 3 = AlCl 3 + 3Н 2 О (7)
Cреди реакций соединения следует особым образом отметить следующие: замещения (5), обмена (6), и как частный случай реакции обмена – реакцию нейтрализации (7).
К реакциям замещения относятся такие, при осуществлении которой атомы простого вещества замещают атомы одного из элементов в сложном веществе. В примере (5) атомы цинка замещают из раствора СuCl 2 атомы меди, при этом цинк переходит в растворимую соль ZnCl 2 , а медь выделяется из раствора в металлическом состоянии.
К реакциям обмена относятся такие реакции, при которых два сложных вещества обмениваются своими составными частями. В случае реакции (6) растворимые соли AgNO 3 и КCl при сливании обоих растворов образуют нерастворимый осадок соли AgCl. При этом они обмениваются своими составными частями – катионами и анионами. Катионы калия К + присоединяются к анионам NO 3 , а катионы серебра Ag + – к анионам Cl - .
К особому, частному случаю, реакций обмена относится реакция нейтрализации. К реакциям нейтрализации относятся такие реакции, в процессе которых кислоты реагируют с основаниями, в результате образуется соль и вода. В примере (7) соляная кислота HCl , реагируя с основанием Al(OH) 3 образует соль AlCl 3 и воду. При этом катионы алюминия Al 3+ от основания обмениваются с анионами Сl - от кислоты. В итоге происходит нейтрализация соляной кислоты.
К реакциям разложения относятся такие, при котором из одного сложного образуются два и более новых простых или сложных веществ, но более простого состава. В качестве реакций можно привести такие, в процессе которых разлагаются 1). Нитрат калия (КNO 3) с образованием нитрита калия (КNO 2) и кислорода (O 2); 2). Перманганат калия (KMnO 4): образуются манганат калия (К 2 МnO 4), оксид марганца (MnO 2) и кислород (O 2); 3). Карбонат кальция или мрамор ; в процессе образуются углекислый газ (CO 2) и оксид кальция (СаО)
2КNO 3 = 2КNO 2 + O 2 (8)
2KMnO 4 = К 2 МnO 4 + MnO 2 + O 2 (9)
СаCO 3 = CaO + CO 2 (10)
В реакции (8) из сложного вещества образуется одно сложное и одно простое. В реакции (9) – два сложных и одно простое. В реакции (10) – два сложных вещества, но более простых по составу
Разложению подвергаются все классы сложных веществ:
1). Оксиды: оксид серебра 2Ag 2 O = 4Ag + O 2 (11)
2). Гидроксиды: гидроксид железа 2Fe(OH) 3 = Fe 2 O 3 + 3H 2 O (12)
3). Кислоты: серная кислота H 2 SO 4 = SO 3 + H 2 O (13)
4). Соли: карбонат кальция СаCO 3 = СаO + CO 2 (14)
5). Органические вещества: спиртовое брожение глюкозы
С 6 Н 12 О 6 = 2С 2 Н 5 ОH + 2CO 2 (15)
Согласно другой классификации, все химические реакции можно разделить на два типа: реакции, идущие с выделением теплоты, их называют экзотермические, и реакции, идущие с поглощением теплоты – эндотермические. Критерием таких процессов является тепловой эффект реакции. Как правило, к экзотермическим реакциям относятся реакции окисления, т.е. взаимодействия с кислородом, например сгорание метана :
СН 4 + 2O 2 = СО 2 + 2Н 2 О + Q (16)
а к эндотермическим реакциям – реакции разложения, уже приводимые выше (11) – (15). Знак Q в конце уравнения указывает на то, выделяется ли теплота в процессе реакции (+Q) или поглощается (-Q):
СаCO 3 = СаO+CO 2 - Q (17)
Можно так же рассматривать все химические реакции по типу изменения степени окисления, участвующих в их превращениях элементов. К примеру, в реакции (17) участвующие в ней элементы не меняют свои степени окисления:
Са +2 C +4 O 3 -2 = Са +2 O -2 +C +4 O 2 -2 (18)
А в реакции (16) элементы меняют свои степени окисления:
2Mg 0 + O 2 0 = 2Mg +2 O -2
Реакции такого типа относятся к окислительно-восстановительным . Они будут рассматриваться отдельно. Для составления уравнений по реакциям такого типа необходимо использовать метод полуреакций и применять уравнение электронного баланса.
После приведения различных типов химических реакций, можно приступать к принципу составлений химических уравнений, иначе, подбору коэффициентов в левой и правой их частях.
Механизмы составления химических уравнений.
К какому бы типу ни относилась та или иная химическая реакция, её запись (химическое уравнение) должна соответствовать условию равенства количества атомов до реакции и после реакции.
Существуют такие уравнения (17), которые не требуют уравнивания, т.е. расстановки коэффициентов. Но в большинстве случаях, как в примерах (3), (7), (15), необходимо предпринимать действия, направленные на уравнивание левой и правой частей уравнения. Какими же принципами необходимо руководствоваться в таких случаях? Существует ли какая ни будь система в подборе коэффициентов? Существует, и не одна. К таковым системам относятся:
1). Подбор коэффициентов по заданным формулам.
2). Составление по валентностям реагирующих веществ.
3). Составление по степеням окисления реагирующих веществ.
В первом случае полагается, что нам известны формулы реагирующих веществ как до реакции, так и после. К примеру, дано следующее уравнение:
N 2 + О 2 →N 2 О 3 (19)
Принято считать, что пока не установлено равенство между атомами элементов до реакции и после, знак равенства (=) в уравнении не ставится, а заменяется стрелкой (→). Теперь приступим к собственно уравниванию. В левой части уравнения имеются 2 атома азота (N 2) и два атома кислорода (О 2), а в правой – два атома азота (N 2) и три атома кислорода (О 3). По количеству атомов азота его уравнивать не надо, но по кислороду необходимо добиться равенства, поскольку до реакции их участвовало два атома, а после реакции стало три атома. Составим следующую схему:
до реакции после реакции
О 2 О 3
Определим наименьшее кратное между данными количествами атомов, это будет «6».
О 2 О 3
\ 6 /
Разделим это число в левой части уравнения по кислороду на «2». Получим число «3», поставим его в решаемое уравнение:
N 2 + 3О 2 →N 2 О 3
Так же разделим число «6» для правой части уравнения на «3». Получим число «2», так же поставим его в решаемое уравнение:
N 2 + 3О 2 → 2N 2 О 3
Количества атомов кислорода и в левой и в правой частях уравнения стали равны, соответственно по 6 атомов:
Но количество атомов азота в обеих частях уравнения не будут соответствовать друг другу:
В левой – два атома, в правой – четыре атома. Следовательно, что бы добиться равенства, необходимо удвоить количество азота в левой части уравнения, поставив коэффициент «2»:
Таким образом, равенство по азоту соблюдено и в целом, уравнение примет вид:
2N 2 + 3О 2 → 2N 2 О 3
Теперь в уравнении можно вместо стрелки поставит знак равенства:
2N 2 + 3О 2 = 2N 2 О 3 (20)
Приведём другой пример. Дано следующее уравнение реакции:
Р + Cl 2 → РCl 5
В левой части уравнения имеется 1 атом фосфора (Р) и два атома хлора (Cl 2), а в правой – один атом фосфора (Р) и пять атомов кислорода (Cl 5). По количеству атомов фосфора его уравнивать не надо, но по хлору необходимо добиться равенства, поскольку до реакции их участвовало два атома, а после реакции стало пять атома. Составим следующую схему:
до реакции после реакции
Cl 2 Cl 5
Определим наименьшее кратное между данными количествами атомов, это будет «10».
Cl 2 Cl 5
\ 10 /
Разделим это число в левой части уравнения по хлору на «2». Получим число «5», поставим его в решаемое уравнение:
Р + 5Cl 2 → РCl 5
Так же разделим число «10» для правой части уравнения на «5». Получим число «2», так же поставим его в решаемое уравнение:
Р + 5Cl 2 → 2РCl 5
Количества атомов хлора и в левой и в правой частях уравнения стали равны, соответственно по 10 атомов:
Но количество атомов фосфора в обеих частях уравнения не будут соответствовать друг другу:
Следовательно, что бы добиться равенства, необходимо удвоить количество фосфора в левой части уравнения, поставив коэффициент «2»:
Таким образом, равенство по фосфору соблюдено и в целом, уравнение примет вид:
2Р + 5Cl 2 = 2РCl 5 (21)
При составлении уравнений по валентностям необходимо дать определение валентности и установить значения для наиболее известных элементов. Валентность – это одно из ранее применяемых понятий, в настоящее время в ряде школьных программ не используется. Но при его помощи легче объяснить принципы составления уравнений химических реакций. Под валентностью понимают число химических связей, которые тот или иной атом может образовывать с другим, или другими атомами . Валентность не имеет знака (+ или -) и обозначается римскими цифрами, как правило, над символами химических элементов, например:
Откуда берутся эти значения? Как их применять при составлении химических уравнений? Числовые значения валентностей элементов совпадают с их номером группы Периодической системы химических элементов Д. И. Менделеева (Таблица 1).

Для других элементов значения валентностей могут иметь иные значения, но никогда не больше номера группы, в которой они расположены. Причём для чётных номеров групп (IV и VI) валентности элементов принимают только чётные значения, а для нечётных – могут иметь как чётные, так и нечётные значения (Таблица.2).

Конечно же, в значениях валентностей для некоторых элементов имеются исключения, но в каждом конкретном случае эти моменты обычно оговариваются. Теперь рассмотрим общий принцип составления химических уравнений по заданным валентностям для тех или иных элементов. Чаще всего данный метод приемлем в случае составления уравнений химических реакций соединения простых веществ, например, при взаимодействии с кислородом (реакции окисления ). Допустим, необходимо отобразить реакцию окисления алюминия . Но напомним, что металлы обозначаются единичными атомами (Al), а неметаллы, находящиеся в газообразном состоянии – с индексами «2» - (О 2). Сначала напишем общую схему реакции:
Al + О 2 →AlО
На данном этапе ещё не известно, какое правильное написание должно быть у оксида алюминия. И вот именно на данном этапе нам на помощь придёт знание валентностей элементов. Для алюминия и кислорода проставим их над предполагаемой формулой этого оксида:
III II
Al О
После чего «крест»-на-«крест» у этих символов элементов поставим внизу соответствующие индексы:
III II
Al 2 О 3
Состав химического соединения Al 2 О 3 определён. Дальнейшая схема уравнения реакции примет вид:
Al+ О 2 →Al 2 О 3
Остаётся только уравнять левую и правую его части. Поступим таким же способом, как в случае составления уравнения (19). Количества атомов кислорода уравняем, прибегая к нахождению наименьшего кратного:
до реакции после реакции
О 2 О 3
\ 6 /
Разделим это число в левой части уравнения по кислороду на «2». Получим число «3», поставим его в решаемое уравнение. Так же разделим число «6» для правой части уравнения на «3». Получим число «2», так же поставим его в решаемое уравнение:
Al + 3О 2 → 2Al 2 О 3
Что бы добиться равенства по алюминию, необходимо скорректировать его количество в левой части уравнения, поставив коэффициент «4»:
4Al + 3О 2 → 2Al 2 О 3
Таким образом, равенство по алюминию и кислороду соблюдено и в целом, уравнение примет окончательный вид:
4Al + 3О 2 = 2Al 2 О 3 (22)
Применяя метод валентностей, можно прогнозировать, какое вещество образуется в процессе химической реакции, как будет выглядеть его формула. Допустим, в реакцию соединения вступили азот и водород с соответствующими валентностями III и I. Напишем общую схему реакции:
N 2 + Н 2 → NН
Для азота и водорода проставим валентности над предполагаемой формулой этого соединения:
Как и прежде «крест»-на-«крест» у этих символов элементов поставим внизу соответствующие индексы:
III I
N Н 3
Дальнейшая схема уравнения реакции примет вид:
N 2 + Н 2 → NН 3
Уравнивая уже известным способом, через наименьшее кратное для водорода, равное «6»,получим искомые коэффициенты, и уравнение в целом:
N 2 + 3Н 2 = 2NН 3 (23)
При составлении уравнений по степеням окисления реагирующих веществ необходимо напомнить, что степенью окисления того или иного элемента называется число принятых или отданных в процессе химической реакции электронов. Степень окисления в соединениях в основном, численно совпадает со значениями валентностей элемента. Но отличаются знаком. Например, для водорода валентность равна I, а степень окисления (+1) или (-1). Для кислорода валентность равна II, а степень окисления (-2). Для азота валентности равны I,II,III,IV,V, а степени окисления (-3), (+1), (+2), (+3), (+4), (+5) и т.д. Степени окисления наиболее часто применяемых в уравнениях элементов, приведены в таблице 3.

В случае реакций соединения принцип составления уравнений по степеням окисления такой же, как и при составлении по валентностям. Например, приведём уравнение реакции окисления хлора кислородом, в которой хлор образует соединение со степенью окисления +7. Запишем предполагаемое уравнение:
Cl 2 + О 2 → ClО
Поставим над предполагаемым соединением ClО степени окисления соответствующих атомов:
Как и в предыдущих случаях установим, что искомая формула соединения примет вид:
7 -2
Cl 2 О 7
Уравнение реакции примет следующий вид:
Cl 2 + О 2 → Cl 2 О 7
Уравнивая по кислороду, найдя наименьшее кратное между двумя и семи, равное «14», установим в итоге равенство:
2Cl 2 + 7О 2 = 2Cl 2 О 7 (24)
Несколько иной способ необходимо применять со степенями окисления при составлении реакций обмена, нейтрализации, замещения. В ряде случаев предоставляется затруднительным узнать: какие соединения образуются при взаимодействии сложных веществ?
Как узнать: что получится в процессе реакции?
Действительно, как узнать: какие продукты реакции могут возникнут в ходе конкретной реакции? К примеру, что образуется при взаимодействии нитрата бария и сульфата калия?
Ва(NО 3) 2 + К 2 SO 4 → ?
Может быть ВаК 2 (NО 3) 2 + SO 4 ? Или Ва + NО 3 SO 4 + К 2 ? Или ещё что-то? Конечно же, в процессе этой реакции образуются соединения: ВаSO 4 и КNО 3 . А откуда это известно? И как правильно написать формулы веществ? Начнём с того, что чаще всего упускается из вида: с самого понятия «реакция обмена». Это значит, что при данных реакциях вещества меняются друг с другом составными частями. Поскольку реакции обмена в большинстве своём осуществляются межу основаниями, кислотами или солями, то частями, которыми они будут меняться, являются катионы металлов (Na + , Mg 2+ ,Al 3+ ,Ca 2+ ,Cr 3+), ионов Н + или ОН - , анионов – остатков кислот, (Cl - , NO 3 2- ,SO 3 2- , SO 4 2- , CO 3 2- , PO 4 3-). В общем виде реакцию обмена можно привести в следующей записи:
Kt1An1 + Kt2An1 = Kt1An2 + Kt2An1 (25)
Где Kt1 и Kt2 – катионы металлов (1) и (2), а An1 и An2 – соответствующие им анионы (1) и (2). При этом обязательно надо учитывать, что в соединениях до реакции и после реакции на первом месте всегда устанавливаются катионы, а анионы – на втором. Следовательно, если в реакцию вступит хлорид калия и нитрат серебра , оба в растворённом состоянии
KCl + AgNO 3 →
то в процессе её образуются вещества KNO 3 и AgClи соответствующее уравнение примет вид:
KCl + AgNO 3 =KNO 3 + AgCl (26)
При реакциях нейтрализации протоны от кислот (Н +) будут соединяться с анионами гидроксила (ОН -) с образованием воды (Н 2 О):
НCl + КОН = КCl + Н 2 O (27)
Степени окисления катионов металлов и заряды анионов кислотных остатков указаны в таблице растворимости веществ (кислот, солей и оснований в воде). По горизонтали приведены катионы металлов, а по вертикали – анионы кислотных остатков.

Исходя из этого, при составлении уравнения реакции обмена, необходимо вначале в левой его части установить степени окисления принимающих в этом химическом процессе частиц. Например, требуется написать уравнение взаимодействия между хлоридом кальция и карбонатом натрия.Составим исходную схему этой реакции:
СаCl + NаСО 3 →
Са 2+ Cl - + Nа + СО 3 2- →
Совершив уже известное действие «крест»-на-«крест», определим реальные формулы исходных веществ:
СаCl 2 + Nа 2 СО 3 →
Исходя из принципа обмена катионами и анионами (25), установим предварительные формулы образующихся в ходе реакции веществ:
СаCl 2 + Nа 2 СО 3 → СаСО 3 + NаCl
Над их катионами и анионами проставим соответствующие заряды:
Са 2+ СО 3 2- + Nа + Cl -
Формулы веществ записаны правильно, в соответствии с зарядами катионов и анионов. Составим полное уравнение, уравняв левую и правую его части по натрию и хлору:
СаCl 2 + Nа 2 СО 3 = СаСО 3 + 2NаCl (28)
В качестве другого примера приведём уравнение реакции нейтрализации между гидроксидом бария и ортофосфорной кислотой:
ВаОН + НРО 4 →
Над катионами и анионами проставим соответствующие заряды:
Ва 2+ ОН - + Н + РО 4 3- →
Определим реальные формулы исходных веществ:
Ва(ОН) 2 + Н 3 РО 4 →
Исходя из принципа обмена катионами и анионами (25), установим предварительные формулы образующихся в ходе реакции веществ, учитывая, что при реакции обмена одним из веществ обязательно должна быть вода:
Ва(ОН) 2 + Н 3 РО 4 → Ва 2+ РО 4 3- + Н 2 O
Определим правильную запись формулы соли, образовавшейся в процессе реакции:
Ва(ОН) 2 + Н 3 РО 4 → Ва 3 (РО 4) 2 + Н 2 O
Уравняем левую часть уравнения по барию:
3Ва (ОН) 2 + Н 3 РО 4 → Ва 3 (РО 4) 2 + Н 2 O
Поскольку в правой части уравнения остаток ортофосфорной кислоты взят дважды, (РО 4) 2 , то слева необходимо также удвоить её количество:
3Ва (ОН) 2 + 2Н 3 РО 4 → Ва 3 (РО 4) 2 + Н 2 O
Осталось привести в соответствие количество атомов водорода и кислорода в правой части у воды. Так как слева общее количество атомов водорода равно 12, то справа оно так же должно соответствовать двенадцати, поэтому перед формулой воды необходимо поставить коэффициент «6» (поскольку в молекуле воды уже имеется 2 атома водорода). По кислороду так же соблюдено равенство: слева 14 и справа 14. Итак, уравнение имеет правильную форму записи:
3Ва (ОН) 2 + 2Н 3 РО 4 → Ва 3 (РО 4) 2 + 6Н 2 O (29)
Возможность осуществления химических реакций
Мир состоит из великого множества веществ. Неисчислимо так же количество вариантов химических реакций между ними. Но можем ли мы, написав на бумаге то или иное уравнение утверждать, что ему будет соответствовать химическая реакция? Существует ошибочное мнение, что если правильно расставить коэффициенты в уравнении, то оно будет осуществимо и на практике. Например, если взять раствор серной кислоты и опустить в него цинк , то можно наблюдать процесс выделения водорода:
Zn+ H 2 SO 4 = ZnSO 4 + H 2 (30)
Но если в этот же раствор опустить медь, то процесс выделения газа наблюдаться не будет. Реакция не осуществима.
Cu+ H 2 SO 4 ≠
В случае, если будет взята концентрированная серная кислота, она будет реагировать с медью:
Cu + 2H 2 SO 4 = CuSO 4 + SO 2 + 2Н 2 O (31)
В реакции (23) между газами азотом и водородом наблюдается термодинамическое равновесие, т.е. сколько молекул аммиака NН 3 образуется в единицу времени, столько же их и распадётся обратно на азот и водород. Смещение химического равновесия можно добиться повышением давления и понижением температуры
N 2 + 3Н 2 = 2NН 3
Если взять раствор гидроксида калия и прилить к нему раствор сульфата натрия , то никаких изменений наблюдаться не будет, реакция будет не осуществима:

КОН + Na 2 SO 4 ≠
Раствор хлорида натрия при взаимодействии с бромом не будет образовывать бром, несмотря на то, что данная реакция может быть отнесена к реакции замещения:
NаCl + Br 2 ≠
В чём же причины таких несоответствий? Дело в том, что оказывается недостаточно только правильно определять формулы соединений , необходимо знать специфику взаимодействия металлов с кислотами, умело пользоваться таблицей растворимости веществ, знать правила замещения в ряду активности металлов и галогенов. В этой статье излагаются только самые основные принципы как расставить коэффициенты в уравнениях реакций , как написать молекулярные уравнения , как определить состав химического соединения.
Химия, как наука, чрезвычайно разнообразна и многогранна. В приведённой статье отражена лишь малая часть процессов, происходящих в реальном мире. Не рассмотрены типы , термохимические уравнения, электролиз, процессы органического синтеза и многое, многое другое. Но об этом в следующих статьях.
сайт, при полном или частичном копировании материала ссылка на первоисточник обязательна.



